La primera celda galvánica del mundo fue desarrollada por Luigi Galvani. Descubre su historia. en este artículoEn esencia, es una fuente temporal de corriente eléctrica generada por una reacción química. El flujo de electrones se genera por la interacción entre dos metales diferentes. Como resultado, la energía química se convierte en energía eléctrica, que puede utilizarse en la vida cotidiana.
Una celda galvánica de concentración es una fuente de corriente que consta de dos electrodos metálicos idénticos colocados en una mezcla de sales de este metal en diversas concentraciones.
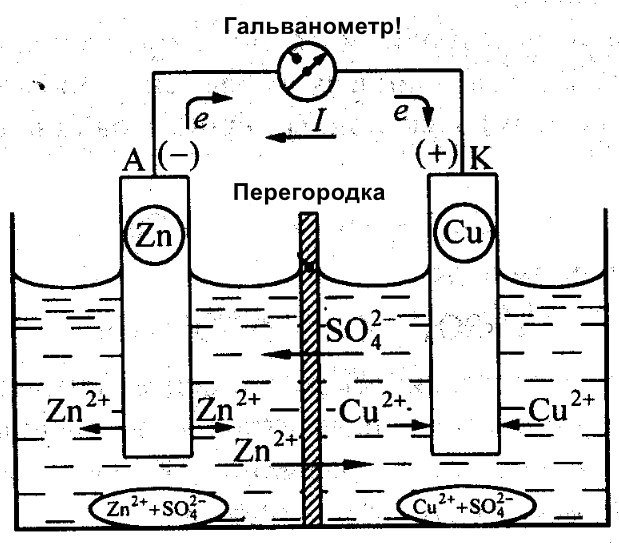
Además de Galvani, Daniel Jacobi también trabajó en la creación de una batería eficiente. Modificó ligeramente su fuente de energía. Esta consiste en una placa de cobre colocada en CuSO₄ y una placa de zinc sumergida en ZnSO₄. Para evitar que interactúen directamente, se coloca una pared porosa entre ellas. A continuación se muestra un diagrama de la celda galvánica de Daniel Jacobi.
El zinc y el cobre tienen diferente reactividad, por lo que su carga será distinta. En consecuencia, los niveles de los electrodos tampoco son uniformes. Esto les permite moverse y generar una corriente eléctrica o galvánica. Esta corriente comienza a fluir cuando una persona o el inventor de un dispositivo de almacenamiento de corriente conecta una carga. Esta carga podría ser una bombilla, una radio, un ratón de ordenador u otros dispositivos eléctricos.
Diagrama esquemático de una celda galvánica
Un diagrama de circuito se refiere a su composición y estructura. Puede construirse a partir de varios elementos químicos mediante dispositivos auxiliares. A continuación, se describe brevemente la estructura de una celda galvánica. Lea más sobre ello en este artículo.!
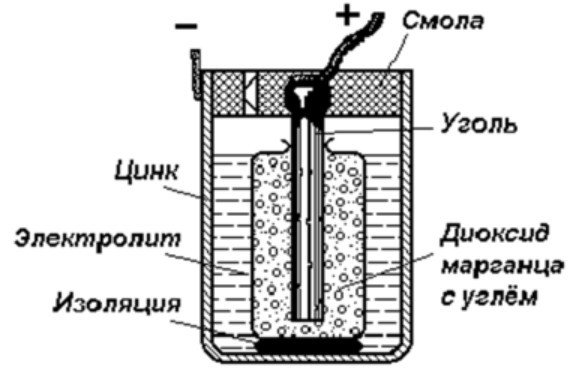
La estructura de una celda galvánica
El dispositivo de almacenamiento de energía más simple consta de:
- Varilla de carbón.
- Dos metales diferentes.
- Electrólito.
- Resina o plástico.
- Aislador.
Como se puede ver en este diagrama, una celda galvánica consta de un electrodo negativo y uno positivo. Pueden estar hechas de cobre, zinc u otros metales. Se denominan celdas de cobre-zinc. A veces se les llama... pilas secas.
Designación de una celda galvánica en un diagrama Se compone de dos líneas verticales, próximas entre sí y a poca distancia. Una de ellas será más pequeña. En los bordes de cada línea hay señales que indican polaridadLa línea larga está marcada como positiva y la corta como negativa. El voltaje puede aparecer junto a ella. Esto significa que el circuito que usa la batería solo funciona con ese voltaje.
El principio de funcionamiento de una celda galvánica
Una celda galvánica funciona mediante el movimiento de electrones de un contacto metálico a otro. Se produce una transformación química. Lea más sobre la termodinámica de una celda galvánica y la formación de electricidad galvánica. Aquí.
Respuestas a preguntas frecuentes
| Galvánico | Explicación |
| Batería | Una fuente de energía que opera mediante procesos que ocurren en un espacio reducido y reducido. En concreto, la energía se genera mediante una reacción química. |
| Celda voltaica o pila voltaica | Este es un elemento energético creado por primera vez por un científico llamado Volt. |
| Proceso | La interacción entre elementos químicos que da lugar a la formación de una corriente eléctrica. |
| Descargar | Esto es la finalización de una reacción química. Es decir, no habrá interacción entre sustancias. La descarga galvánica está presente en Warframe. Esencialmente, es una modificación escasa. Se usa en armas cuerpo a cuerpo. PolaridadVersión 2. |
| Contacto galvánico | Este es el contacto entre los electrodos y la solución. |
| Efecto | La aparición de una diferencia entre dos contactos hechos de dos tipos de metal. La magnitud depende de la temperatura y la composición química de los conductores. En esencia, esta es la primera ley de Volta. |
| Conexión/enlace/cadena | Conectar dos o más secciones de un circuito eléctrico a una fuente de corriente. |
| Carga galvánica | Llenando la batería de energía. |
La galvanización es un proceso químico que utiliza corriente eléctrica. Esta reacción reduce la cantidad de cationes metálicos disueltos hasta tal punto que forman una capa uniforme sobre un electrodo metálico. Como resultado, el artículo se vuelve más duradero, desaparecen las pequeñas abolladuras y su apariencia se vuelve más atractiva.
Tipos de celdas galvánicas
Hay varios tipos específicos de baterías.
Tabla de celdas galvánicas
| Tipo | Voltaje | Principales ventajas |
| Litio | 3 V | Grande capacidad, alta corriente. |
| Baterías de sal o carbono-zinc | 1,5 pulgadas | El más barato. |
| Níquel oxihidroxilado NiOOH | 1,6 voltios | Alta corriente. Alta capacidad. |
| Alcalino o alcalino | 1,6 V | Alta corriente. Buen volumen. |
Este tema se trata con más detalle en el artículo. tipos de baterías!
Propósito de una celda galvánica
Está diseñado para arrancar equipos eléctricos. Estos pueden incluir:
- Mirar.
- Controles remotos.
- Linternas.
- Equipo médico.
- Computadoras portátiles.
- Juguetes.
- Llaveros.
- Teléfonos.
- Punteros láser.
- Calculadoras.
Y cosas similares a nuestro alrededor.
Celda galvánica en casa
Puedes fabricar una fuente de alimentación sencilla tú mismo. Para ello, necesitarás los siguientes materiales:
- Vaso de plástico.
- Electrolito. Puede ser una solución salina, bicarbonato o ácido cítrico diluido en agua.
- Placas de dos metales diferentes. Por ejemplo, aluminio y cobre.
- Cables
Proceso de fabricación
Toma un vaso de plástico y vierte el electrolito. No lo llenes hasta el borde; es mejor dejarlo a 1 o 2 centímetros de distancia. Conecta los cables a las placas metálicas. A continuación, coloca las placas de cobre y aluminio en los bordes del recipiente. Deben estar paralelas entre sí. Una vez listo, puedes medir el voltaje con un voltímetro.
Conecte el dispositivo y toque las sondas con los contactos de la fuente de alimentación. Manténgalas en su lugar hasta que la pantalla muestre voltaje. Normalmente, es de 0,5 a 0,7 voltios. Estos valores dependen del electrolito, o más precisamente, de la sustancia utilizada como electrolito.
Así se hace una celda galvánica casera.