El uso generalizado de pequeños electrodomésticos por parte de los consumidores implica la necesidad de fuentes de energía o circuitos de alimentación única. celdas galvánicas, comúnmente conocidas como baterías. Aparecieron por primera vez en 1800, gracias al físico italiano Alessandro Volta. Varían en tamaño, forma, voltaje, capacidad y tipo de batería. Las baterías alcalinas y salinas se utilizan ampliamente en el mercado de pequeños electrodomésticos y electrónica.
¿Qué son las baterías salinas?
Baterías de sal — Fuentes de corriente eléctrica generadas en un dispositivo simple mediante una reacción química. A veces se denominan baterías de carbono-zinc o baterías de carbono. Este tipo de celda se considera el más económico, pero tiene una baja densidad energética, lo que la hace ideal para dispositivos de baja potencia. En dispositivos con alto consumo de energía o con picos característicos de corriente de carga y temperatura, su vida útil es corta y, por lo tanto, no se utilizan.
Designación de baterías de sal
La denominación de baterías salinas se acepta según varias normas:
- Sistema de clasificación americano.
- Sistema internacional (IEC).
- Norma interestatal (GOST).
| Sistema de clasificación estadounidense | Clasificación Internacional IEC | GOST | Tamaño, mm | Capacidad, mAh |
| A | R23 | 17x50 | ||
| Automóvil club británico | R6 | 316 | 14,5 x 50,5 | 1100 |
| AAA | R03 | 286 | 10,5 x 44,5 | 540 |
| do | R14 | 343 | 26,2x50 | 3800 |
| D | R20 | 373 | 34,2 x 61,5 | 8000 |
| F | R25 | 33x91 | ||
| 1/2AA | R14250 | 312 | 14,5 x 25 | 250 |
| R10 | R10 | 332 | 21,5 x 37,3 | 1800 |
Por ejemplo, la marca de una batería salina R 6 significa: redonda, cilíndrica, dedo, elemento tipo sal, dimensiones totales 14,5x50,5, capacidad1100 mAh. El voltaje estándar es de 1,5 V. La designación "R" (sal) en la etiqueta de la batería distingue las baterías salinas de otros tipos de baterías (alcalinas o de litio).
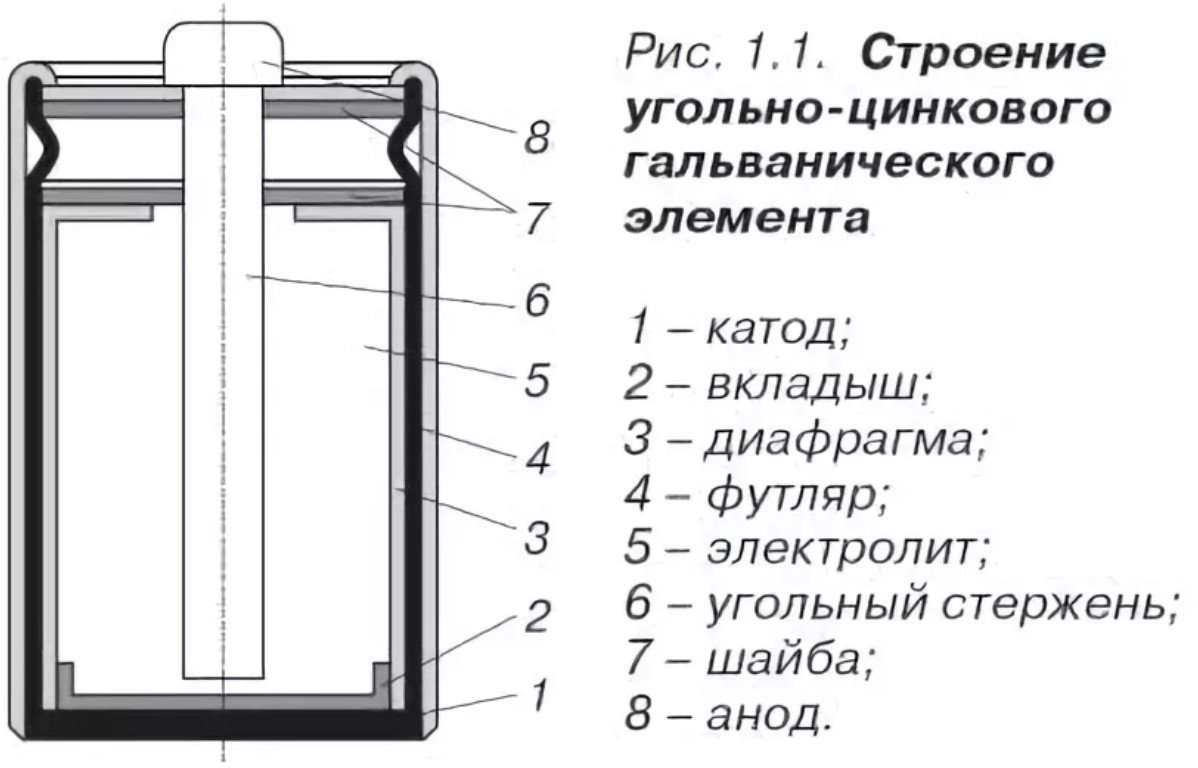
Diseño y composición
El diseño de una batería de sal es bastante simple y consta de:
- Cátodo - lo mismo El caso de la batería de sal está hecho Fabricado en zinc, con propiedades anticorrosivas mejoradas y un alto grado de purificación (menos).
- El ánodo es un aglomerado, fabricado por prensado, impregnado con electrolito (plus).
- Electrolito: cloruro de amonio o cloruro de zinc, con la adición de un espesante (almidón).
- Conductor de corriente de carbono: pasa por el centro y está tratado con una composición de parafina.
- Cámara de gas: situada en la parte superior, diseñada para recoger los gases de la reacción química.
- Junta: ubicada en la parte superior, actúa como sellador.
- Estuche protector: cartón o lata para proteger contra la corrosión y fugas de electrolitos.
Consideremos la composición de una batería salina desde un punto de vista químico:
- El cátodo es de zinc altamente purificado, resistente a la corrosión.
- Ánodo - mezcla de MnO2, grafito, impregnación electrolítica.
- El electrolito es cloruro de amonio o una mezcla de cloruro de zinc con cloruro de calcio.
¿Qué pilas son mejores: salinas (1) o alcalinas (2)?
La comparación se puede realizar en forma de tabla, donde se ven claramente las ventajas y desventajas de los diferentes tipos de elementos:
| Parámetros de comparación | 1 | 2 |
| Condiciones de temperatura, condiciones de funcionamiento | El rendimiento se reduce a bajas temperaturas y no puede soportar picos de corriente. | Funciona bien a bajas temperaturas, hasta -20Oh, resisten fácilmente las sobretensiones, no temen un aumento brusco de la corriente de carga |
| Consumir preferentemente antes de | 2-3 años | 5 años |
| Solicitud | Adecuado para su uso en dispositivos con bajo consumo de corriente. | Adecuado para su uso en equipos con consumo energético medio y alto. |
| Instrumentos, dispositivos técnicos | Despertadores, relojes de pared, mandos a distancia, mini linternas, juguetes sencillos. | Reproductores, linternas, juguetes musicales, grabadoras de voz, tensiómetros |
Al elegir una fuente de alimentación para un dispositivo con requisitos operativos específicos, es importante saber distinguir entre una batería salina y una alcalina. Mientras que las baterías salinas se identifican con la letra R, las alcalinas van precedidas de la letra L (LR).
Conclusiones y recomendaciones
Este tipo de fuente de alimentación es más ligera y económica. Sin embargo, la vida útil de las baterías salinas es corta (de 2 a 3 años) y pueden autodescargarse parcialmente durante el almacenamiento y el uso, debido a una sobrecarga repentina de corriente. Por lo tanto, dado su bajo rendimiento y su bajo costo, es fácil adquirir varios juegos de baterías como respaldo.
No alto capacidadLas baterías de sal (2-3 veces menos que otros tipos) limitan su uso a dispositivos simples con baja corriente de carga.
Es fácil determinar si es posible cargar baterías salinas: el nombre de la batería está indicado en el cuerpo del dispositivo destinado a cargar. capacidadEn mAh. Si no dispone de este valor, se trata de una batería normal y, a pesar de los numerosos consejos de expertos, no debería cargarse. Cargarla no proporcionará el efecto esperado a largo plazo y podría provocar un accidente por sobrecalentamiento y fuga de electrolito. Si necesita una fuente de alimentación más fiable y duradera, es mejor invertir en una alternativa alcalina o en una batería recargable.
Dato interesante: Batería de sal casera Se puede hacer de forma muy sencilla. Necesitarás monedas de 50 kopeks, papel de aluminio, papel y una solución salina. Es recomendable remojar las monedas en una solución de vinagre antes de usarlas para eliminar cualquier placa o suciedad. Ensamble el dispositivo: una moneda, papel empapado en la solución salina y papel de aluminio. Repita este proceso varias veces, creando una columna con la moneda (positiva) en un extremo y el papel de aluminio (negativo) en el otro. La corriente se genera por la diferencia de potencial creada por el electrolito (solución salina) entre el metal del papel de aluminio y la moneda. Este invento se llama pila voltaica, y su voltaje depende directamente del número de monedas utilizadas: cuantas más monedas haya, mayor será el voltaje obtenido. Sin embargo, después del experimento, las monedas ya no se pueden usar; tendrán una capa oxidada.